作用機序
オシメルチニブはEGFR(Epidermal Growth Factor Receptor:上皮成長因子受容体)チロシンキナーゼ阻害薬の一種です。そもそも EGFRは細胞表面に存在する受容体であり、EGF(上皮成長因子)が結合することで細胞内部のチロシンキナーゼによるシグナルが細胞内に伝わり、細胞の増殖が調節されています。がん細胞では、EGFRが異常に活性化され、がん細胞が増殖する原因となっています。
非小細胞肺がんではEGFRの活性を担うキナーゼ領域内にdel19変異(エクソン19欠損変異)か、L858R変異を有しています。また、残りの約10%の患者さんではexon20挿入変異やG719X、L747P、S768Iといった変異が低頻度に見つかることが知られています。なおdel19変異とL858R変異をcommon mutationと呼び、これ以外をuncommon mutationと言います。これらの変異が異常なシグナル伝達の原因となります。
そこで変異のあるEGFRを阻害すれば腫瘍増殖シグナルを抑制できます。オシメルチニブは細胞内部のチロシンキナーゼを阻害することで腫瘍増殖シグナルを遮断します。
このとき正常細胞に存在するEGFRには作用しないよう設計されています。オシメルチニブは正常細胞に発現したEGFRには影響を及ぼさず、遺伝子変異のある遺伝子変異のあるEGFRを狙って阻害する特徴があります。
また従来のEGFR阻害薬であるゲフィチニブなどでは耐性化が問題となっていました。これはEGFR遺伝子エクソン20の790番目のスレオニン(T)がメチオニン(M)に置換されることで起ことが原因でした。しかしオシメルチニブはT790M変異のあるEGFRにも作用するよう開発された薬剤です。
オシメルチニブの耐性(C797S、MET増幅)
オシメルチニブ治療後の約10〜20%でC797S耐性変異という別の遺伝子変異が出現し、数年以内に再発することがあります。C797S耐性変異は薬剤結合ポケットの構造が変化し、オシメルチニブが結合できなくなります。
また耐性ができる経路は複数あり、その一つにMET増幅があります。これはEGFRを介さずに増殖シグナルが細胞に伝わってしまう経路が新たにできてしまうことを意味します。MET増幅のあるEGFR陽性非小細胞肺がんに対してテポチニブ(テプミトコ)を併用することで抗腫瘍効果が認められています(INSIGHT2試験)
同効薬
| 世代 | 成分名 | 商品名 |
| 第1世代 | ゲフェチニブ | イレッサ |
| 第1世代 | エルロチニブ | タルセバ |
| 第2世代 | ジオトリフ | アファチニブ |
| 第2世代 | ダコミチニブ | ビジンプロ |
| 第3世代 | オシメルチニブ | タグリッソ |
添付文書・適正使用ガイド・ガイドラインのポイント
ここからは添付文書や適正使用ガイドラインで注目すべきポイントについて簡単に説明していきます。まずオシメルチニブ(タグリッソ)の適応は以下の2つになります。
- EGFR遺伝子変異陽性の手術不能又は再発非小細胞肺癌
- EGFR遺伝子変異陽性の非小細胞肺癌における術後補助療法(2022年適応追加)
用法・用量
1日1回80mgを経口投与します。ただし術後補助療法の場合、投与期間は36ヶ月までと記載されています。また減量基準に該当する場合は1日1回40mgを経口投与します。添付文書では「間質性肺炎」「QT延長」「その他の副作用」について休薬や減量の目安が記載されています。
相互作用(食事やPPI)
オシメルチニブは高脂肪食摂取後に投与してもCmaxやAUCに影響がないため服用タイミングに規定はありません。しかしエルロチニブやアファチニブは食事の影響により吸収率が低下するため空腹時に服用しなければいけません。
またCYP3A4により代謝されるためCYP3A4阻害薬による血中濃度上昇が懸念されますが、影響は小さく臨床上問題となることはほとんどありません。
一方でCYP3A4誘導薬については影響を受け、オシメルチニブの血中濃度が減少し効果が減弱する可能性がります。そのため添付文書では「CYP3A4誘導作用のない薬剤への代替を考慮すること」と記載があります。
またQT延長を起こす薬剤と併用することでQT延長リスクが増強する可能性があります。そうした薬剤を併用する場合は定期的な心電図検査や電解質検査の重要性が高まります。
制酸剤、喫煙、UGT、トランスポーターの影響は他のEGFR-TKIで問題となることがありますが、オシメルチニブに関しては影響はありません。
一次治療・二次治療
一次治療(ファーストライン)とは、手術不可能ながんに対して抗がん剤治療する場合の最初の抗がん剤治療のことです。つまり添付文書の適応としては「EGFR遺伝子変異陽性の手術不能又は再発非小細胞肺癌」についての説明になります。
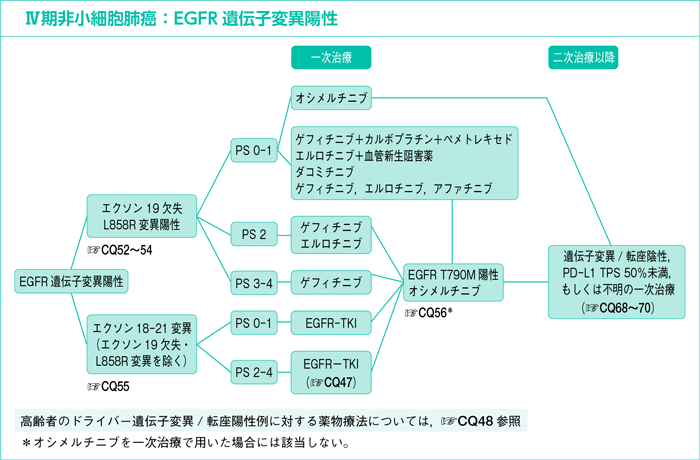
出典:肺癌診療ガイドライン
上記図を確認すると、一次治療にオシメルチニブを使用すると他のEGFR-TKIに戻ることは一般的ではありません。逆にゲフィチニブなどのEGFR-TKIを一次治療で使用した場合はオシメルチニブに変更するルートがあります。
術後補助療法
ADAURA試験の優れた結果により、2022年に術後補助療法の適応が追加されました。しかし、添付文書には次のように記載されています。「病理病期IB期(AJCC/UICC 第7版)の患者に対する有効性及び安全性は確立していない。」 このコメントの理由は、ADAURA試験全体では良好な結果が得られましたが、参加したIB~ⅢAの患者のうちステージIBのみを解析すると効果が小さい傾向が見られたことや、ステージIBの日本人症例が登録されていなかったことです。そのため、ステージIBの術後補助療法としては適応外になっています。
これを踏まえた上で、肺癌診療ガイドラインを確認してみましょう。ガイドラインでは以下のような術後補助療法が推奨されています。
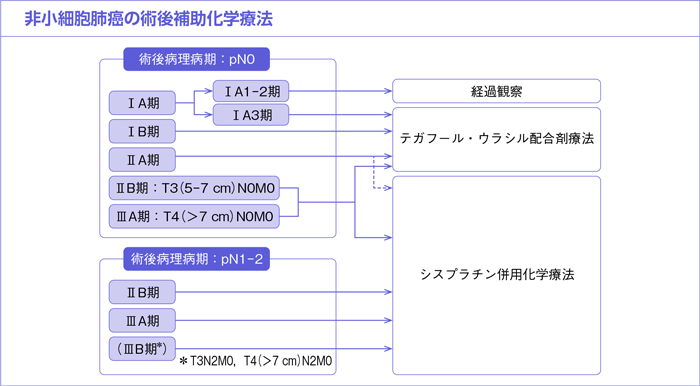
出典:肺癌診療ガイドライン
ここではオシメルチニブについての推奨はありません。またEGFR遺伝子変異陽性肺がんの術後補助療法についての記載は以下のようになります。この記載においてもオシメルチニブの推奨度は強くありません。

出典:肺癌診療ガイドライン
ADAURA試験ではオシメルチニブのプラセボ対象試験だったので、従来の化学療法と比較してどちらが優れているか結論が出ていないため上記のような推奨になっています。添付文書の記載においても「白金系抗悪性腫瘍剤を含む術後補助療法の適応となる場合は、当該治療を終了した患者を対象とすること」とあります。
したがってオシメルチニブによる術後補助療法は従来の化学療法後に追加して服用するケースが多いことを理解しておきましょう。
なお化学療法とタグリッソの比較はNeoADAURA試験によって検証が進められています。比較対照のイメージは以下のようになります。

出典:日本がん対策図鑑
リチャレンジ
副作用
第3世代EGFR-TKIであるオシメルチニブは従来のEGFR-TKIと比較して副作用は少なくなっていますが、間質性肺炎やQT延長などの致死的な副作用が見られるケースがあります。
間質性肺炎
| Grade1 | 臨床症状なし |
| Grade2 | 身の回り以外の日常生活動作の制限 |
| Grade3 | 身の回りの日常生活動作の制限、酸素投与を要する |
| Grade4 | 緊急処置(気管切開や気管内挿管) |
出典:CTCAE ver5.0
薬剤性間質性肺炎は様々な薬剤で起こり得ます。オシメルチニブについても間質性肺炎の報告があるため早期対応が必要になります。まず好発時期は以下のように、投与後6ヶ月以内に集中していることが分かります。
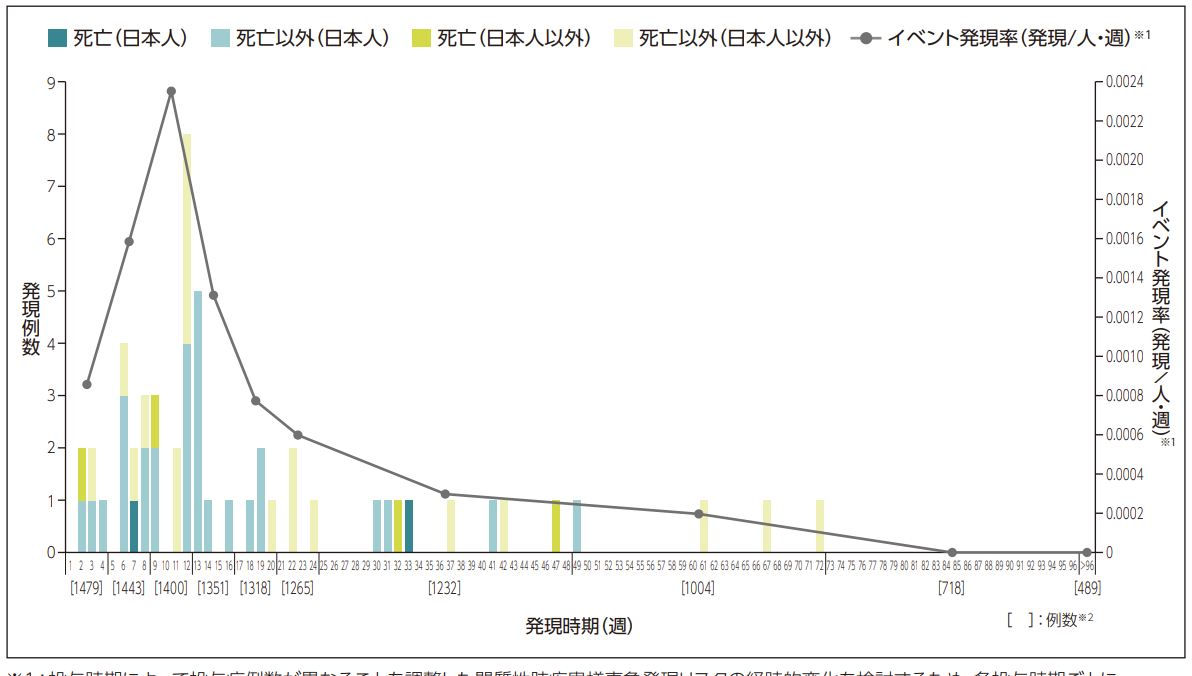
出典:適正使用ガイド
ただし6ヶ月以降での発症も報告されているため初期症状を理解する必要があります。間質性肺炎の症状は風邪に似ており、咳や発熱が現れます。通常の風と異なるポイントは労作時の息切れになります。
続いてレントゲン検査で新たな陰影(すりガラス様陰影)が現れた場合は間質性肺炎を疑い血清マーカー(KL-6、SP-D等)を測定します。流れを図示すると以下のようになります。
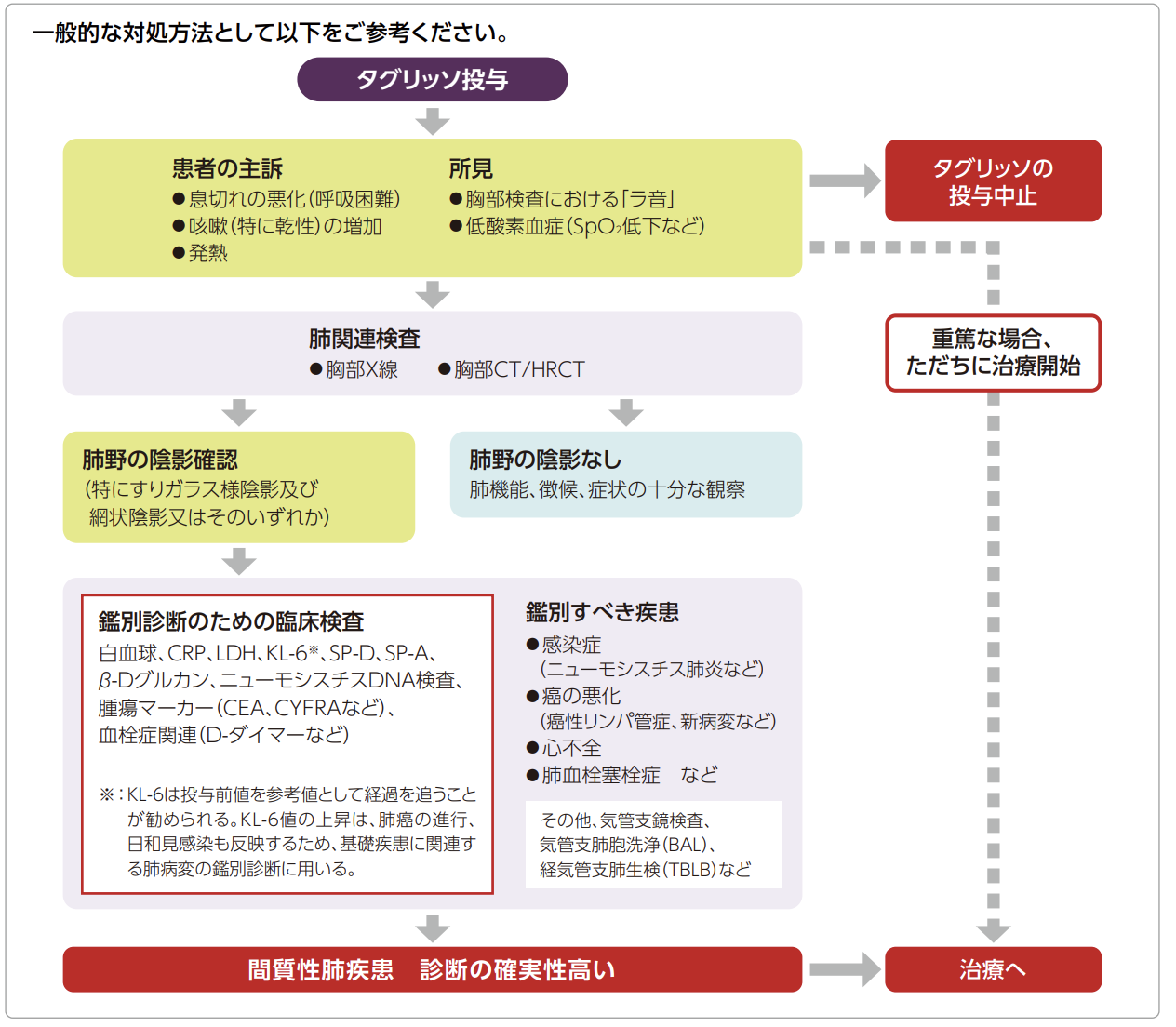
出典:適正使用ガイド
ただし間質性肺炎に特異的な所見は無いため、リスク薬剤の投与時期が事前確率として重要になります。また原因薬剤を注視して自然経過で改善が見られた場合は薬剤性間質性肺炎の可能性が高くなります。
なお免疫チェックポイント阻害薬でも間質性肺炎を起こすことがあります。例えばニボルマブの治療歴がある患者にオシメルチニブを投与して間質性肺炎を起こすケースがあります。そうした症例が複数あるため、安全対策に関する通知(薬生安発0124第1号 薬生安発0124第2号)を発出されています。
QT延長
| Grade1 | 平均QTc450-480ms |
| Grade2 | 平均QTc481-500ms |
| Grade3 | 平均QTc501以上またはベースラインから60ms以上の変化 |
| Grade4 | TdPまたは多型性心室頻拍または重篤な不整脈の症状 |
出典:CTCAE ver5.0
EGFR-TKIではオシメルチニブのみQT延長のリスクが高いことが知られています。QT延長の出現率は1.3%、Grade3以上の発現率は0.1%程度であり、決して頻度は高くありませんが、発症したら死に至ることもあるため忘れてはいけません。QT延長が確認された場合は以下のようなフローチャートを参考に減量・休薬を考慮します。
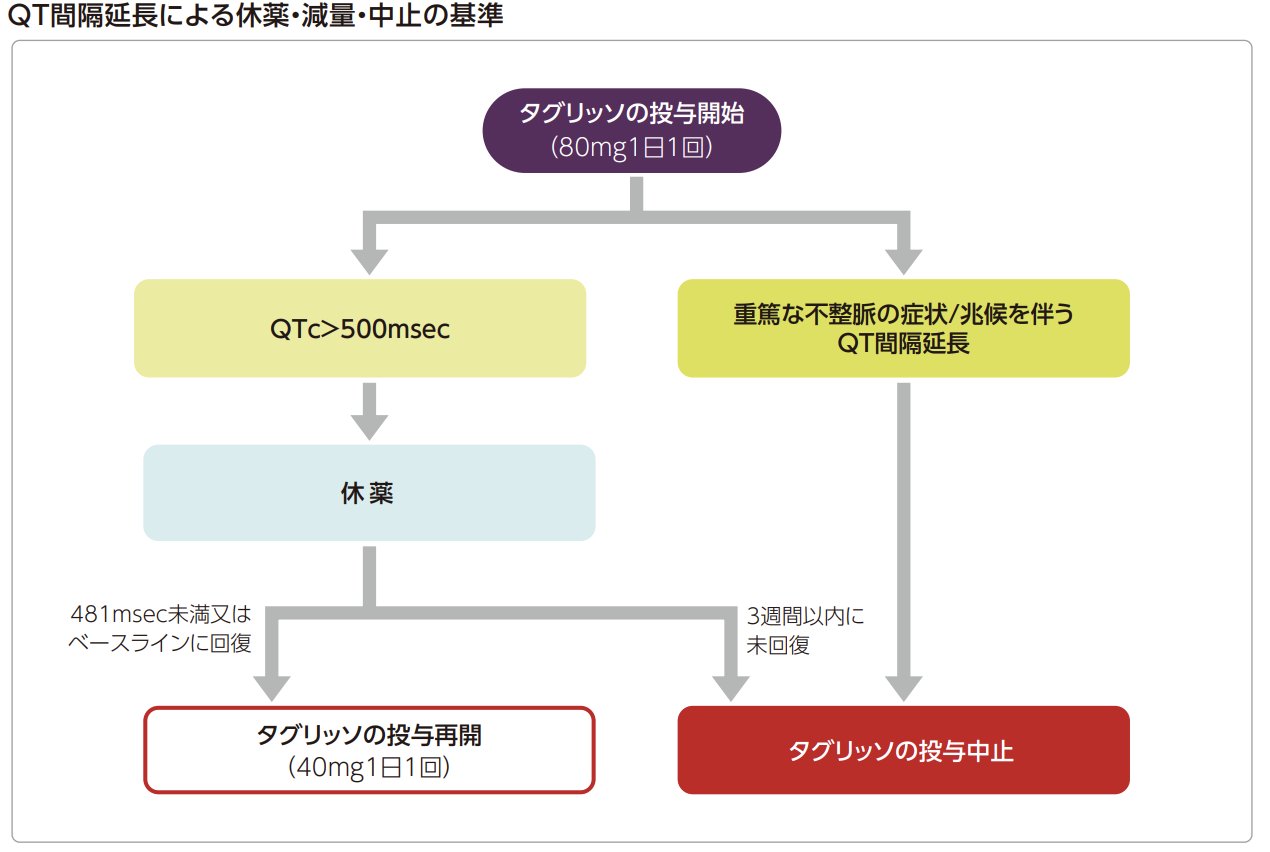
QT延長が起こったとしても自覚症状は無いため、心電図を確認しなければ分かりません。QT延長の怖いポイントはTdP(トルサードポワンツ)に発展する可能性があることです。
TdPは心室頻拍(VT)の一種であり、失神や突然死の原因となります。症状が持続すると心拍数が増加(120以上、200〜250)し、十分な血流が得られないため、めまいや胸の不快感、失神を起こします。また持続時間が長くなると心室細動(VF)に移行して心停止に至ることがあります。
QT延長のリスク要因としては低カリウム血症や遺伝、薬剤性などがあります。薬剤性QT延長のリスクが高い薬剤として抗うつ薬、抗不整脈薬、抗精神病薬などがありますが、特にエスシタロプラム(レクサプロ)はリスクが高くQT延長のある患者に禁忌となっているためオシメルチニブとの併用も避けた方が良いでしょう。
また抗不整脈薬を選択する場合はSicilian Gambit分類を確認すればQT延長のリスクを一覧で把握することができます。緩和領域ではメサドンもQT延長のリスクになることを忘れてはいけません。
心不全(LVEF低下)
オシメルチニブは第1, 2世代のEGFR-TKIと比較してLVEF減少のオッズ比が6.75と高いことが知られています。オシメルチニブによってLVEF低下した場合は中止以外にもゲフェチニブ等に変更する選択肢も考えてよいかもしれません。
なお日本腫瘍循環器学会によるとがん治療関連心機能障害(CTRCD)を次のように定義しています。「がん薬物療法試行中に心不全症状の有無にかかわらず、左室駆出率がベースラインより10%以上低下し、施設基準下限値を下回る状態」
下痢
| Grade1 | 排便回数増加(4回/日未満) |
| Grade2 | 排便回数増加(4〜6回/日) |
| Grade3 | 排便回数増加7回以上 |
| Grade4 | 生命を脅かす、緊急処置が必要 |
出典:CTCAE ver5.0
抗がん剤による下痢は投与直後に発生する早発型と投与後24時間以降に発生する遅発型に分けて考えることができます。遅発性下痢の原因として、抗がん剤や代謝物が腸粘膜上皮を傷つけることにあるとされます。オシメルチニブを含むEGFR-TKIでは遅発性下痢を起こしやすいと言われています。
ASCOガイドラインで推奨されているロペラミドの投与法は、「初回4mg服用し、その後4時間間隔もしくは水様便後に2mgを投与する。そして、12-24時間後に評価を行い、下痢の改善が得られない場合は2時間間隔での投与を考慮する」とされています。
免疫抑制
骨髄抑制による血球減少の頻度は添付文書で次のように記載されています。血小板減少(9.2%)、好中球減少(8.3%)、白血球減少(10.8%)、貧血(4.5%)。殺細胞性抗がん剤と比較すると頻度が少ないことが特徴です。
オシメルチニブの論文・臨床試験
オシメルチニブ+ベバシズマブ(タグリッソ+アバスチン)

出典:日本がん対策図鑑
オシメルチニブ+ラムシルマブ(タグリッソ+サイラムザ)

出典:日本がん対策図鑑
ADAURA
ステージIB~ⅢA患者背景は女性が多い。

出典:日本がん対策図鑑
従来のEGFR-TKIでは術後補助療法としてPFS(無増悪生存期間)を延長する薬剤はありましたが、OS(全生存期間を延長する薬剤はありませんでした。つまりカプランマイヤー曲線が最終的には重なる結果が続いていました。しかし、オシメルチニブでは従来のEGFR-TKIと異なり、OSを延長するという結果が得られました。

出典:日本がん対策図鑑
脳転移
オシメルチニブは血液脳関門を通過するため、脳転移のあるEGFR陽性非小細胞肺がんに対して有効性が示されています。頭蓋内転移に対するオシメルチニブ(タグリッソ®)の有効性と安全性の評価:系統的レビューとメタ解析
